Noutati
Comunicare directa catre profesionistii din domeniul sanatatii privind falsificarea medicamentului Herceptin (trastuzumab) – flacon cu 150 mg pulbere pentru concentrat pentru solutie perfuzabila
Data: 08/05/2014
Serii de fabricaţie:
H4105B01, H4136B02, H4143B01, H4150B01, H4152B04, H4171B01, H4168B02, H4169B01, H4179B02, H4180B01, H4184B01, H4185B02, H4194B01, H4195B01, H4196B01, H4261B01, H4263B02, H4271B01, H4279B01, H4284B04, H4293B01, H4303B01, H4301B09, H4311B07, H4319B02, H4324B03, H4329B01, N1001B01, N1002B02, N1002B03, N1010B02
Stimate profesionist din domeniul sănătăţii,
Compania farmaceutică Roche România S.R.L., reprezentantă a firmei F. Hoffmann-La Roche Ltd. (denumită în continuare Roche), de comun acord cu Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale (ANMDM) şi Agenţia Europeană a Medicamentului (European Medicines Agency, EMA) doreşte să vă informeze în legătură cu următoarele:
Rezumat
- Produse falsificate, etichetate iniţial în limba italiană drept flacoane de medicament Herceptin 150 mg pulbere pentru concentrat pentru soluţie perfuzabilă, au fost găsite la distribuitorii din Marea Britanie, pentru a fi distribuite mai departe în afara teritoriului Marii Britanii, și în Finlanda, Germania, Austria şi Suedia. Există posibilitatea ca eticheta şi ambalajul exterior originale în limba italiană să fi fost înlocuite cu etichete şi ambalaje în limba naţională.
- Etichetele flacoanelor suspectate ca fiind falsificate şi ambalajul exterior original sunt inscripţionate cu serii de fabricaţie autentice, însă este posibil ca seriile de pe etichetele flacoanelor să nu corespundă celor de pe ambalajul exterior. În plus, unele flacoane pot conţine lichid în loc de pulbere sau pot prezenta semne de deschidere anterioară.
- Produsele falsificate nu trebuie utilizate deoarece nu pot fi considerate nici sigure, nici eficace.
- Dacă sunteţi în posesia unui produs pe care îl suspectaţi de falsificare ori a cărui autenticitate nu o puteţi confirma sau dacă suspectaţi posibilitatea ca unui pacient să i se fi administrat un medicament falsificat, trebuie să contactaţi imediat Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale.
- Nu se anticipează ca aceasta să determine un deficit de aprovizionare cu acest medicament pentru pacienţi.
Informaţii suplimentare
Compania Roche a fost informată recent în legătură cu descoperirea în Germania a unor produse confirmate a fi falsificate, etichetate drept flacoane cu medicament Herceptin 150 mg pulbere pentru concentrat pentru soluţie perfuzabilă (trastuzumab). Alte flacoane suspecte au fost depistate în Marea Britanie (pentru a fi distribuite mai departe în alte țări), Finlanda, Austria şi Suedia. Produsele falsificate au aceleaşi serii de fabricaţie ca şi produsele din seriile de medicament Herceptin autentice ale companiei Roche. Conform informaţiilor pe care le deţinem în prezent, un importator paralel german a cumpărat produsele suspecte de la doi distribuitori din Marea Britanie, care le-au achiziţionat la rândul acestora de la distribuitori italieni. În Italia, compania Roche furnizează medicamentul numai către farmaciile din spitale, conform legislaţiei naţionale, ceea ce înseamnă că distribuitorii italieni nu au fost aprovizionaţi de către compania Roche Italia.
Analiza chimică a confirmat că minim unul dintre produsele falsificate NU conţine trastuzumab (pulbere), substanţa activă a medicamentului Herceptin, ci ceftriaxonă (pulbere), un antibiotic din clasa cefalosporinelor.
Alte flacoane conţin un lichid în locul pulberii de culoare albă spre galben pal şi prezintă semne de deschidere anterioară (a se vedea exemplele de mai jos). Compoziţia acestui lichid nu a fost stabilită în toate cazurile, însă poate conţine trastuzumab diluat.
Toate produsele falsificate trebuie considerate nesterile, chiar dacă par intacte.
Produsele falsificate nu trebuie utilizate, deoarece nu pot fi considerate nici sigure, nici eficace.
Inspecţie vizuală
Produsul falsificat poate arăta identic cu medicamentul Herceptin autentic sau nu.
Diferenţa dintre produsele falsificate depistate până în prezent şi medicamentul Herceptin autentic s-a stabilit pe baza unei combinaţii a următoarelor caracteristici:
- etichetele de pe flacoane şi cutii sunt în limba italiană (este posibil ca distribuitorii să fi reetichetat şi reambalat ulterior produsul, iar textul să fie în limba naţională);
- seriile de fabricaţie enumerate mai sus;
- seriile de fabricație și data expirării inscripționată pe eticheta flaconului nu corespunde, în unele cazuri cu cea inscriționată pe cutie
- prezenţa unei etichete autocolante „bollini” (vezi mai jos), specific pentru ambalajele expediate în Italia.
- prezintă semne de manipulare anterioară a capacului (capacul nu este fixat corespunzător sau este deteriorat).
- prezenţa unui lichid în flacon (Herceptin 150 mg pulbere pentru concentrat pentru soluţie perfuzabilă este o pulbere de culoare albă spre galben pal).
- dopul a fost deja perforat.
Exemple de cutii falsificate:
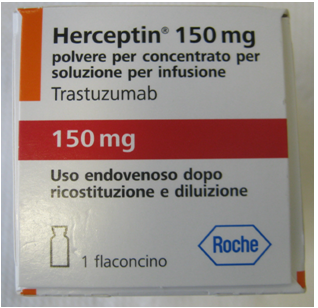

Exemple de flacoane falsificate:
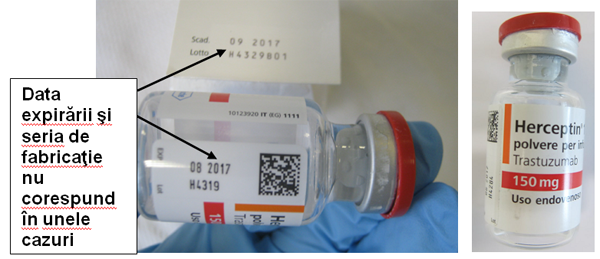
Posibile riscuri pentru pacienţi
- Produsele falsificate pot fi considerate ca lipsite de eficacitate terapeutică. Tratamentul pacienţilor care suferă de cancer mamar, HER2-pozitiv sau cancer gastric poate fi serios afectat sau întârziat (spre exemplu, dacă se omite astfel un ciclu complet de tratament eficace).
- Dacă pacientului i se administrează ceftriaxonă în loc de trastuzumab, acesta poate manifesta reacţiile adverse asociate cu antibioticul în cauză, care sunt enumerate în informaţiile despre medicamentul respectiv.
- Lipsa sterilităţii poate duce la infecţii, cu risc de afecţiuni severe la pacienţii cu afecţiuni maligne şi imunosupresie.
- Există posibilitatea apariţiei altor reacţii adverse cauzate de un lichid cu o compoziţie necunoscută.
Acţiuni necesare din partea profesionistului din domeniul sănătăţii
Dacă sunteţi în posesia unui produs pe care îl suspectaţi de falsificare ori a cărui autenticitate nu o puteţi confirma sau dacă suspectaţi posibilitate ca unui pacient să i se fi administrat un medicament falsificat, trebuie să contactaţi imediat Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale, la adresa:
Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale,
Str. Aviator Sănătescu, Nr. 48, Sector 1, Bucureşti, România,
Tel: + 4 0757 117 259
Fax: +4 0213 163 497
e-mail: cringuta.braiescu@anm.ro; contrafacere@anm.ro
În plus, trebuie să contactaţi Persoana Responsabilă cu Asigurarea Calităţii din cadrul companiei Roche România S.R.L., la adresa:
Farm. Cristian Buzoianu
Qualified Person
ROCHE ROMÂNIA S.R.L.
Piaţa Presei Libere, Nr. 3-5
Clădirea City Gate – Turnul de Sud
Departamentul Comercial, etaj 6
013702, Sector 1
Bucureşti, România
Recepţie: +4021 206 47 01/02/03
Fax: +4021 206 47 00
Produsul suspectat de falsificare trebuie păstrat pentru cercetări ulterioare.
Dacă aveţi cunoştinţă despre faptul că un pacient manifestă orice fel de reacţii adverse care consideraţi că se pot corela cu administrarea medicamentului Herceptin sau cu utilizarea ceftriaxonei sau că prezintă reacţii adverse diferite de cele asociate, de obicei, cu administrarea medicamentului Herceptin, inclusiv absenţa oricărui efect, vă rugăm să vă adresaţi imediat Persoanei Responsabile cu Farmacovigilenţa din cadrul companiei Roche România S.R.L.:
Dr. Florentina Halici
Drug Safety Manager
ROCHE ROMANIA S.R.L.
Piaţa Presei Libere, Nr. 3-5, Clădirea City Gate – Turnul de Sud
Departamentul Medical, etaj 6, 013702, Sector 1
Bucureşti, România
Telefon direct: +4021 206 47 48
Recepţie: +4021 206 47 01/02/03
Fax: +4021 206 47 00
e-mail: romania.drug_safety@roche.com
Compania Roche colaborează cu autorităţile competente din domeniul sănătăţii şi cu organele de aplicare a legii în vederea sprijinirii activităţilor de cercetare întreprinse pentru stabilirea sursei de provenienţă a medicamentului falsificat şi prevenirea distribuirii sale ulterioare. Cu toate acestea, compania nu are autoritatea oficială de intervenţie directă şi nu îşi va asuma responsabilitatea în cazul revendicărilor de despăgubiri referitoare la produsele falsificate. Compania Roche a implementat o serie de măsuri tehnice de combatere a falsificării, care implică design‑ul, ambalajul şi etichetarea propriilor produse, colaborând totodată cu autorităţile competente în vederea instituirii unui sistem de urmărire şi trasabilitate a produselor din lanţul de distribuţie până la momentul eliberării în farmacii.
Compania Roche recomandă, în mod ferm, ca achiziţionarea medicamentului Herceptin şi a produselor Roche în general, în vederea utilizării pentru indicaţiile aprobate, să se facă exclusiv din surse autorizate.
Cu stimă,
Dr. Ileana Popescu
Director Medical
Roche România S.R.L.
Pentru întrebări şi informaţii suplimentare, vă rugăm să contactaţi Departamentul Medical al companiei ROCHE ROMÂNIA S.R.L.:
Dr. Florentina Halici
Drug Safety Manager
ROCHE ROMÂNIA S.R.L.
Piaţa Presei Libere, Nr. 3-5
Clădirea City Gate – Turnul de Sud
Departamentul Medical, etaj 6, 013702, Sector 1
Bucureşti, România
Telefon direct: +4021 206 47 48
Recepţie: +4021 206 47 01/02/03
Fax: +4021 206 47 00
NOUTATI!
11
APR
APR
22
MAR
MAR

